Szukasz informacji o raku dróg żółciowych?
Tutaj znajdziesz najważniejsze informacje dotyczące tego nowotworu.
Szukasz informacji o raku dróg żółciowych? Tutaj znajdziesz najważniejsze informacje dotyczące tego nowotworu.
Mapa Diagnostyki i Leczenia Raka Dróg Żółciowych
O raku dróg żółciowych
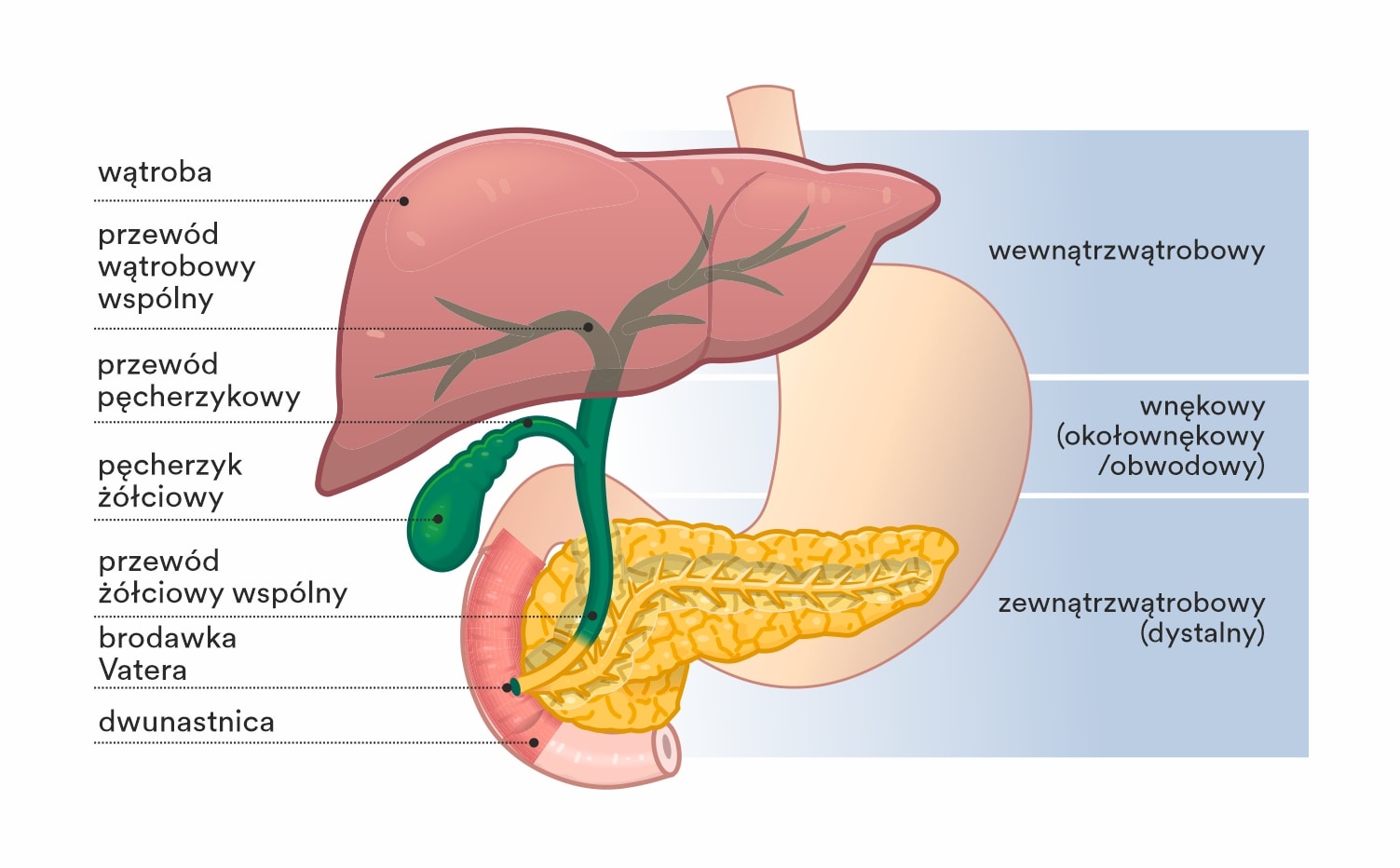
Rak dróg żółciowych (łac. cholangiocarcinoma) jest pierwotnym nowotworem wątroby. Powstaje w nabłonku wyścielającym światło dróg żółciowych, które służą do odprowadzania żółci z wątroby do dwunastnicy. Rak może rozwijać się także wyłącznie w nabłonku pęcherzyka żółciowego (Łac. Carcinoma vesicae fellae), który jest zbiornikiem żółci wydzielanej przez wątrobę. Mówi się o nim, że to mały narząd z poważnymi chorobami.
Klasyfikacja raka dróg żółciowych zależy od odcinka przewodu żółciowego, w którym rozwinęła się choroba. Obejmuje ona trzy kategorie:
- rak wewnątrzwątrobowych dróg żółciowych — powstaje w przewodach żółciowych w wątrobie,
- postać wnękowa i obwodowa raka dróg żółciowych — powstaje w bezpośrednim sąsiedztwie wątroby, obejmując miejsce podziału przewodu wątrobowego wspólnego na prawy i lewy,
- rak zewnątrzwątrobowych dróg żółciowych lub dalszych odcinków — powstaje w dowolnym odcinku przewodu żółciowego wspólnego, poza wątrobą.
Epidemiologia
Rak dróg żółciowych jest rzadko rozpoznawaną chorobą nowotworową. Rocznie w Polsce diagnozę słyszy ok. 800 osób. U 8 na 10 pacjentów choroba diagnozowana jest już zbyt późno, w zaawansowanym, nieoperacyjnym stadium.
Profilaktyka
Profilaktyka i badania kontrolne odgrywają dużą rolę we wczesnym wykrywaniu nowotworów, ale są pomocne jedynie tam, gdzie opracowano proste testy skriningowe – np.: mammografia i USG w raku piersi, niskoemisyjna tomografia w raku płuc, cytologia w raku szyjki macicy, badanie PSA w diagnostyce raka prostaty. W przypadku nowotworów dróg żółciowych i pęcherzyka nie ma jeszcze określonych takich badań.
Dlatego tak ważne jest reagowanie na sygnały wysyłane przez nasz organizm, kontrolne wizyty u lekarza oraz regularne wykonywanie podstawowych badań kontrolnych, do których należą m.in.: podstawowe badania profilaktyczne: morfologia, OB, stężenie glukozy we krwi, próby wątrobowe oraz badanie ogólne moczu, USG jamy brzusznej. Badania należy wykonywać od razu jeśli są dolegliwości, a kontrolnie najlepiej raz w roku/co 2 lata.

Podstawowe badania profilaktyczne: morfologia, OB, stężenie glukozy we krwi oraz badanie ogólne moczu

USG jamy brzusznej
Szczególną uwagę powinni zwracać na ryzyko wystąpienia raka dróg żółciowych pacjenci, u których zdiagnozowano nawracające zapalenia pęcherzyka żółciowego, polipy w pęcherzyku żółciowym i kamicę pęcherzyka żółciowego i dróg żółciowych, oraz stwardniające zapalenie dróg żółciowych (PSCW ) – w ich przypadku czujność onkologiczna ma szczególną wartość.
Czynniki ryzyka
Nowotwory dróg żółciowych są rzadkie i nie do końca znane są czynniki ryzyka ich rozwoju. Zwiększone ryzyko rozwoju nowotworów dróg żółciowych zauważa się u osób otyłych, z rozpoznanym zespołem metabolicznym tj. otyłość brzuszna, palących papierosy, nadużywających alkoholu, zakażonych wirusami WZW (wirusowym zapaleniem wątroby) typu B i C.

Otyłość brzuszna

Palenie papierosów

Nadużywanie alkoholu

Wirusowe zapalenie wątroby
Dodatkowo ryzyko to znacząco zwiększa się
u osób chorujących na:
Cukrzycę
Marskość wątroby
Kamienie dróg żółciowych
Stłuszczenie wątroby
Zespół Carolego
dziedziczną chorobę charakteryzującą się obecnością licznych torbieli wewnątrzwątrobowych dróg żółciowych
Torbiele cholechodalne
charakteryzują się pojedynczymi lub mnogimi zmianami, stanowiącymi odcinkowe poszerzenia wewnątrzwątrobowe bądź zewnątrzwątrobowe dróg żółciowych o kształcie kulistym lub workowatym
Zapalenie trzustki
Choroby zapalne jelit
Polipy w pęcherzyku żółciowym
Motylicę wątrobową
groźny pasożyt – przywra, która powoduje w organizmie człowieka i zwierząt chorobę pasożytniczą zwaną fascjolozą; zazwyczaj bytuje w wątrobie i drogach żółciowych żywiciela; prowadzi do niebezpiecznych powikłań
Pierwotne stwardniające zapalenie dróg żółciowych
przewlekłą chorobę wątroby, w której dochodzi do zastoju żółci w drogach żółciowych na skutek postępującego włóknienia, niszczenia i zwężenia wewnątrzwątrobowych i zewnątrzwątrobowych dróg żółciowych
Jeśli występuje u Ciebie jedno lub kilka z wyżej wymienionych schorzeń oznacza to, że możesz być narażona/y na raka dróg żółciowych i obligatoryjnie powinnaś/powinieneś regularnie wykonywać badania kontrolne pozwalające na wczesne wykrycie ewentualnych zmian nowotworowych w drogach żółciowych i wątrobie.
Objawy

Żółtaczka

Ciemny mocz

Jasny stolec

Żółtaczka

Ciemny mocz

Jasny stolec

Żółtaczka

Ciemny mocz

Jasny stolec

Ból brzucha

Gorączka

Swędzenie

Nudności
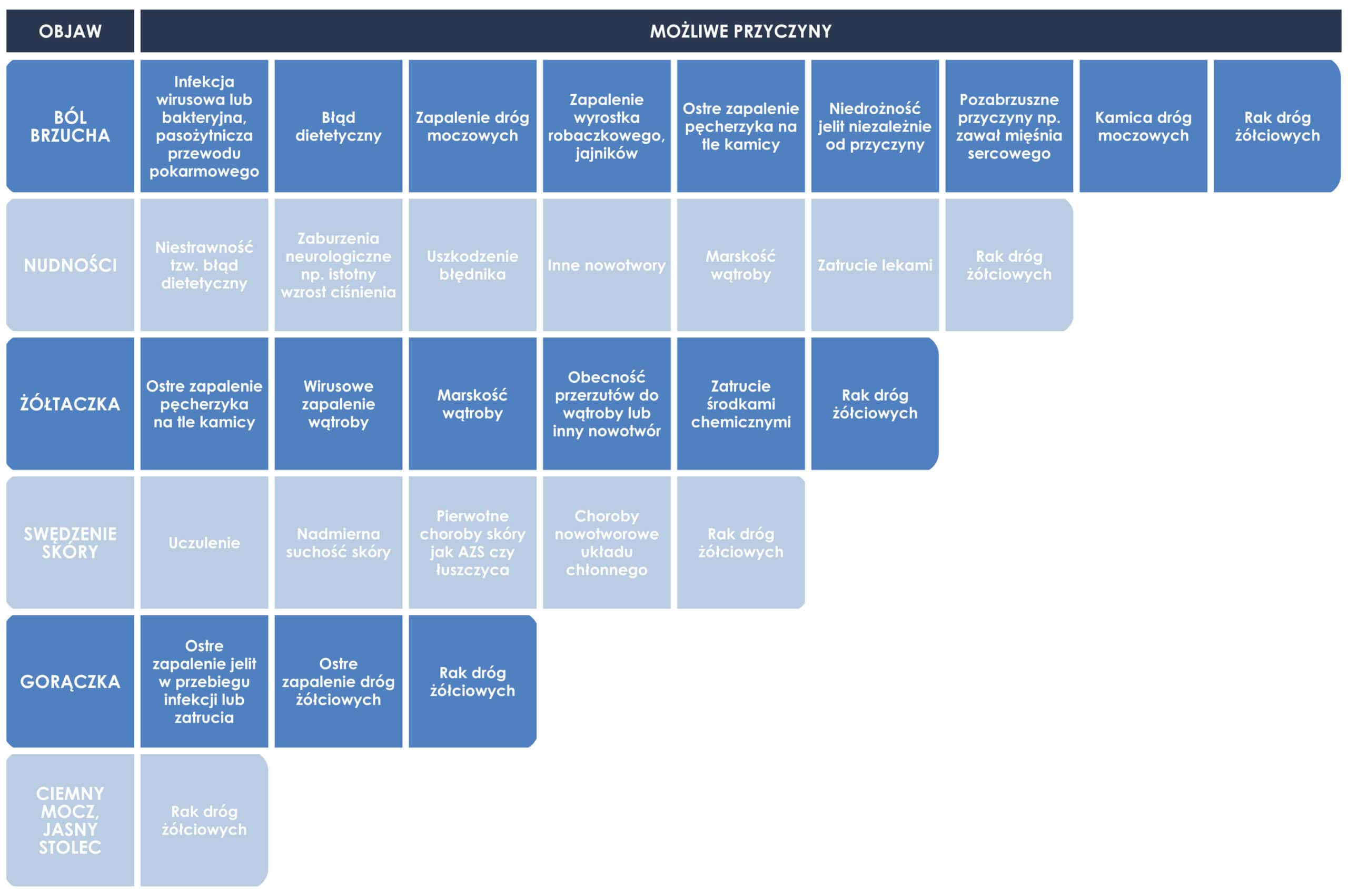
Rak dróg żółciowych i pęcherzyka żółciowego na wczesnym etapie rozwoju często jest bezobjawowy. Większość guzów wykrywana jest dopiero w zaawansowanym stadium choroby lub przypadkowo podczas rutynowego USG. Zmiany nowotworowe wywołują różne objawy:
- zespół objawów dyspeptycznych: nudności, wymioty, pobolewania w jamie brzusznej,
- nagłe pojawienie się żółtaczki bez poprzedzającego bólu,
- niekiedy objawom zarówno dyspeptycznym jak i żółtaczce może towarzyszyć gorączka. Do rozwoju żółtaczki dochodzi gdy guz blokuje przewód żółciowy na dowolnym odcinku i dochodzi do zatrzymania przepływu żółci do jelita cienkiego. Gromadząca się żółć odkłada się w tkankach powodując zażółcenia skóry, a w pierwszej kolejności białek oczu, taki stan nazywamy żółtaczką. Zażółcenie bez poprzedzającego napadu bółu – żółtaczką mechaniczną. Mocz również przybiera ciemnożółtą barwę, a stolec ma jasny kolor. Żółtaczce może towarzyszyć również swędzenie skóry.
Pojawienie się żółtaczki jest wskazaniem do pilnego zgłoszenia się do lekarza. Jeśli zażółcenie pojawiło się po napadzie bólu należy zgłosić się do chirurga, jeśli towarzyszy zażółceniu gorączka należy udać się do oddziału ratunkowego celem określenia. Może być wskazana pilna operacja lub antybiotykoterapia. W innych przypadkach udaj się do lekarza rodzinnego celem rozpoczęcia diagnostyki, w tym wykluczenia wirusowego zapalenia wątroby, które może również powodować żółtaczkę.
Jeśli w pęcherzyku żółciowym są kamienie to często utożsamiane jest to z jedyną przyczyną występujących objawów, podczas gdy rak nie rozwija się w pęcherzyku, a w drogach żółciowych wewnątrzwątrobowych.
Nie bagatelizuj dolegliwości, ponieważ mogą one świadczyć o pewnych zaburzeniach, które warto zidentyfikować. Im dłużej będziesz zwlekać, tym choroba będzie bardziej zaawansowana.
Objawy takie jak napad silnego bółu, żółtaczka, gorączka, wyraźna utrata masy ciała samoistna wymagają zgłoszenia do lekarza natychmiast. Objawy pobolewania w jamie brzusznej, nudności, odbarwienia stolca czy ciemnego moczu, dyskomfortu trawiennego należy chwilę obserwować np. 7-10 dni i jeśli nie ustępują samoistnie koniecznie wykonać usg brzucha i zgłosić się do lekarza.
Pamiętaj! Obserwuj swój organizm, ponieważ inne objawy lub nieoczywiste objawy mogą być przyczyną raka dróg żółciowych. Każdy z tych objawów należy zawsze skonsultować z lekarzem, a następnie wykonać podstawowe badania diagnostyczne w celu postawienia wstępnej diagnozy.
Diagnostyka
Podstawowymi badaniami są testy laboratoryjne krwi, a także badania obrazowe – USG jamy brzusznej, dzięki któremu zostanie przeprowadzona wstępna ocena Twojego aktualnego stanu zdrowia aby postarać się okrelić przyczynę dolegliwości. Badanie USG trwa około 15-20 minut i jest bezbolesne. Podejrzenie zmian nowotworowych wymaga rozszerzenia diagnostyki o tomografie komputerową, ECPW oraz biopsję. Te badania pozwalają określić sposób leczenia.
W ramach diagnostyki pogłębionej lekarz skieruje pacjenta na dodatkowe badania. Ich wybór jest uzależniony od klasyfikacji raka dróg żółciowych, a więc umiejscowienia nowotworu.
- ERCP/PTC tj. endoskopowa cholangiopankreatografia wsteczna/przezskórna cholangiografia przezwątrobowa; (opcjonalnie wykonanie biopsji lub cholangioskopii) – czyli badanie pozwalające ocenić niedrożności dróg żółciowych, powinna być pobrana tkanka do diagnozy/klasyfikacji histologicznej i NGS (sekwencjonowanie nowej generacji).
- Magnetyczny rezonans jądrowy, w tym MRCP tj. cholangiopankreatografia rezonansu magnetycznego – czyli dokładna ocena miejscowego zajęcia p/dCCA (dystalny rak dróg żółciowych/proksymalny (okołownękowy) rak dróg żółciowych), w tym dróg żółciowych i anatomii naczyń oraz identyfikację przerzutów do wątroby.
- Tomografia komputerowa klaki piersiowej + jamy brzusznej + miednicy – celem oceny stopnia zaawansowania nowotworu w celu wykrycia miejscowej/odległej limfadenopatii (tj. powiększenia węzłów chłonnych) i choroby przerzutowej. Obecność przerzutów w wątrobie pozwala na wykonanie biopsji celowanej gruboigłowej – co jest bardzo pomocne w diagnostyce i pozwala także na następowe badania molekularne guza.
- PET-CT – czyli pozytonowa tomografia emisyjna, która może pozwolić na identyfikację przerzutów do węzłów chłonnych, przerzutów odległych i nawrotu choroby.
Klasyfikacja TNM raka dróg żółciowych
TNM oznacza Tumour (guz), Node (węzły chłonne) i Metastasis (przerzuty).
T
określa wielkość guza pierwotnego
N
określa zajęcie okolicznych węzłów chłonnych
M
określa, czy nowotwór rozsiał się do innych części ciała (przerzuty)
Po wykonaniu diagnostyki pogłębionej i ocenie stanu zaawansowania choroby,
lekarz onkolog/gastroenterolog przedstawi dalszą ścieżkę postępowania.
Raki te najczęsciej rosną miejscowo, naciekając sąsiednie struktury (wnęka wątroby, dwunastnica, brodawka Vatera) wcześnie dając przerzuty do miąższu wątroby. Raki te rozprzestrzeniają się drogami naczyń krwionośnych i chłonnych, ale zazwyczaj w obszarze jamy brzusznej, rzadko dając przerzuty do odległych miejsc jak np. płuca, mózg.
Z uwagi na fakt, że najczęściej rozpoznawany jest proces zaawansowany, rozlegle naciekający obszar wnęki wątroby lub dwunastnicy i brodawki Vatera nie sposób określić precyzyjnie, w którym odcinku rozpoczął się rozwój guza, decyduje wówczas obraz patomorfologiczny z pobranego wycinka, potwierdzający, że guz wywodzi się z dróg żółciowych.
Leczenie
Rak dróg żółciowych jest poważną, ale też rzadką chorobą. Dlatego niezwykle ważne jest, aby pacjenci byli leczeni przez wykwalifikowanych specjalistów. Leczenie pacjenta powinno zostać omówione podczas konsylium lekarskiego tj. spotkania specjalistów z różnych dziedzin leczenia raka (np. chirurdzy, gastroenterolodzy, radiolodzy, onkolodzy i pielęgniarki onkologiczne), którzy omówią z pacjentem jego stan i ustalą najlepszy sposób opieki i leczenia.
Ważne jest, abyś jako pacjent w pełni uczestniczył w procesie decyzyjnym dotyczącym leczenia. Dzięki temu otrzymasz odpowiednie informacje i możliwość wyboru opieki, która spełnia Twoje potrzeby oraz odzwierciedla ważne dla Ciebie oczekiwania odnośnie całego procesu leczenia.
Zastosowane leczenie raka dróg żółciowych zależy od lokalizacji i wielkości guza
oraz czy doszło do przerzutów poza drogi żółciowe, jak również od ogólnego stanu zdrowia pacjenta.
Operacyjny rak dróg żółciowych
Jeśli zdiagnozowano u Ciebie resekcyjnego raka dróg żółciowych możesz zostać poddany operacji usunięcia zmian nowotworowych wraz z marginesem zdrowej wątroby i węzłami chłonnymi. Po operacji lekarz może zadecydować o włączeniu chemioterapii, terapii celowanej lub terapii skojarzonej.
W tym ostatnim przypadku decyzję, które terapie będą połączone podejmuje lekarz onkolog kliniczny, nazywany przez wielu chemioterapeutą. Jeśli po zastosowanym leczeniu pojawią się przerzuty do węzłów chłonnych lub do innych narządów należy podjąć leczenie systemowe, a po uzyskaniu poprawy można rozważać usunięcie pozostałości.
Zabieg chirurgiczny
Operację wykonuje się celem fizycznego usunięcia guza i jest obecnie jedyną metodą zapewniającą możliwość wyleczenia raka dróg żółciowych. Najczęściej jest to poważna i skomplikowana operacja, ponieważ w momencie diagnozy nowotworu zazwyczaj jest on już bardzo zaawansowany. Decyzja dotycząca możliwości operacyjnego usunięcia nowotworu zależy od wyników badań diagnostycznych oraz od ogólnego stanu zdrowia pacjenta.
- Usunięcie dróg żółciowych
Jeżeli nowotwór jest w bardzo wczesnym stadium, możliwe jest usunięcie tylko dróg żółciowych, w których występuje. Pozostałe przewody wątroby zostają chirurgicznie połączone z jelitem cienkim, co umożliwia ponowny przepływ żółci. - Częściowa resekcja wątroby
Jeżeli nowotwór nacieka na wątrobę, usuwana jest zmieniona chorobowo część wątroby wraz z drogami żółciowymi. - Zabieg Whipple’a
Jeżeli nowotwór nacieka na pobliskie struktury, może zaistnieć konieczność usunięcia dróg żółciowych, części żołądka, części jelita cienkiego (dwunastnicy), trzustki, pęcherzyka żółciowego i regionalnych węzłów chłonnych. - Zabieg chirurgiczny usunięcia niedrożności (zatorów)
Jeżeli zabieg chirurgiczny usunięcia guza jest niemożliwy, być może wskazane będzie wykonanie zabiegu usunięcia zatorów uniemożliwiających normalny przepływ żółci przez przewody. Usunięcie zatoru możliwe jest poprzez wprowadzenie do przewodu rurki (stentu), która zapewni jego drożność. Częściowa niedrożność jelita cienkiego (dwunastnicy) może powodować różne objawy, m.in. wymioty. Rozwiązaniem tego problemu może być chirurgiczne usunięcie niedrożnego odcinka jelita, wykonanie pomostu naczyniowego dwunastnicy i połączenie żołądka z pozostałą częścią jelita cienkiego (jelitem czczym). - Przeszczep wątroby
Całkowite usunięcie wątroby i przewodów żółciowych, a następnie przeszczepienie wątroby jest stosowane u szczegółowo wyselekcjonowanych pacjentów. Z tego powodu przeszczepianie wątroby u chorych z rakiem dróg żółciowych jest wykonywane bardzo rzadko.
Nieoperacyjny rak dróg żółciowych
Jeśli jednak pacjent nie kwalifikuje się ze względu na zaawansowanie choroby lub stan ogólny do zabiegu chirurgicznego, po konsultacji z lekarzem może zostać zakwalifikowany do leczenia systemowego.

Chemioterapia
w tym przypadku wykorzystuje się leki, które mają działanie przeciwnowotworowe (cytotoksyczne). U pacjentów z chorobą nowotworową dróg żółciowych często stosuje się kilka schematów chemioterapii, ale głównie pochodne platyny i gemcytabinę (PG/KG).

TACE
tj. przezcewnikowa chemoembolizacja tętnicza czyli wstrzykiwanie chemioterapeutyku do naczyń doprowadzających krew do guza w celu zmniejszenia dopływu do niego krwi i zniszczenia komórek nowotworowych – niezwykle rzadko stosowana w tym typie raka bo zabieg jest możliwy jeśli jest 1 guz do 3 cm.
Terapia celowana
czyli hamowanie wzrostu nowotworu poprzez stosowanie leku przeciw komórce nowotworowej z określoną zmianą genetyczną (obecnie zarejestrowane 2 terapie : dla mutacji BRCA oraz FGFR2 – w Polsce aktualnie nie są refundowane, ewentualnie wniosek w ramach RDTL tj. ratunkowego dostępu do technologii lekowych).

Immunoterapia
czyli hamowanie wzrostu nowotworu poprzez modyfikację działań układu odpornościowego mające na celu wywołanie odpowiedzi przeciwnowotworowej (terapia obecnie zarejestrowana ale nie refundowana w Polsce, która wg. wytycznych UE i USA powinna być stosowana w I linii leczenia).

Radioterapia
czyli wykorzystywanie promieni rentgenowskich o wysokiej energii służące do zabijania komórek nowotworowych. Nie jest ono stosowane rutynowo w leczeniu raka dróg żółciowych, ale czasami wykorzystuje się je w celu złagodzenia objawów w leczeniu paliatywnym.

Terapia skojarzona
polegająca na łączeniu kilku metod leczniczych u jednego chorego, decyzję, które z dostępnych opcji terapeutycznych będą połączone i podane choremu, podejmuje lekarz onkolog/gastroenterolog.
Po zastosowanym leczeniu lekarz może zakwalifikować pacjenta do operacji usunięcia zmiany nowotworowej wraz z marginesem zdrowej wątroby i węzłów chłonnych jeśli leczenie systemowe zostało podane w intencji zmniejszenia zmian i spowodowało je.
Badania kliniczne
Badanie kliniczne to badanie naukowe prowadzone z udziałem pacjentów, którego celem jest:
- Sprawdzenie nowych metod leczenia,
- Rozważenie nowych połączeń istniejących metod leczenia lub zmiany sposobu ich podawania w celu zwiększenia skuteczności lub zmniejszenia skutków ubocznych,
- Porównanie skuteczności leków stosowanych celem kontrolowania objawów.
W badaniu klinicznym mogą wziąć udział pacjenci spełniający wymagania opisane w protokole, który zatwierdzany jest przez odpowiednie instytucje (w Polsce jest to Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych). Potencjalni uczestnicy mogą zgłosić się do badania klinicznego sami lub zostać zaproszeni przez lekarza.
Po uzyskaniu pełnej informacji i podpisaniu świadomej zgody pacjent przechodzi szereg badania celem sprawdzenia czy spełnione zostają wymagania zawarte we wspomnianym wcześniej protokole (m.in. stopień zaawansowania choroby, choroby współistniejące, przyjmowane leki). Po zakwalifokowaniu pacjenta do badania klinicznego jest on dokładnie monitorowany w jego trakcie i po jego zakończeniu.
Aktualnie prowadzone badania kliniczne nad rakiem dróg żółciowych można wyszukać w Rejestrze Badań Klinicznych Unii Europejskiej.
Mapa ośrodków, w których leczeni są
pacjenci z rakiem dróg żółciowych*
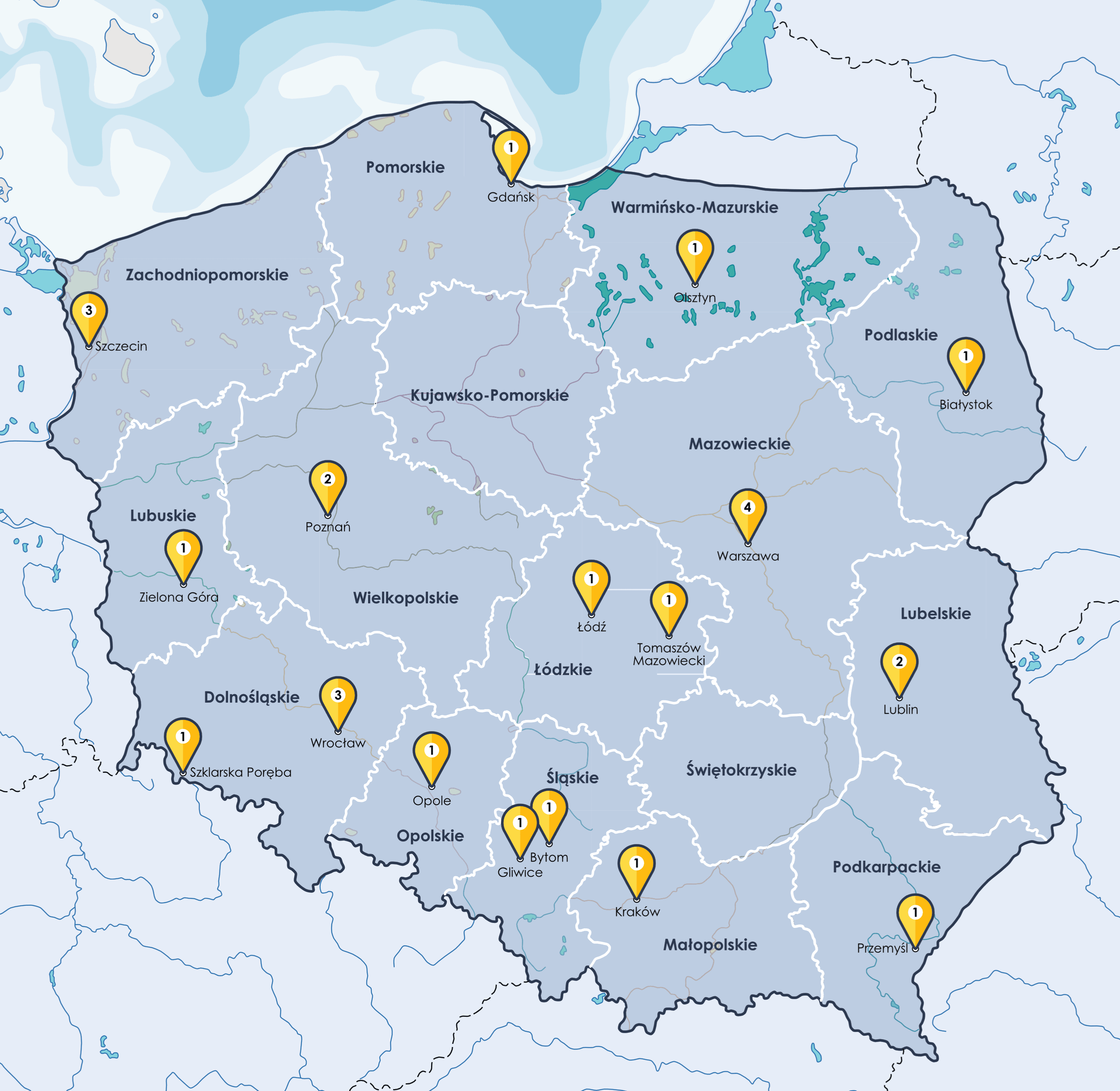
* Ostatnia aktualizacja mapy 05 grudnia 2023
Dane kontaktowe ośrodków
woj. dolnośląskie
4 Wojskowy Szpital Kliniczny z Polikliniką SP ZOZ
ul. Rudolfa Weigla 5, 50-981 Wrocław
tel.: (71) 721 05 55
www.4wsk.pl
Uniwersytecki Szpital Kliniczny
ul. Borowska 213, 50-556 Wrocław
tel.: (71) 733 11 10
www.aszk.wroc.pl
Dolnośląskie Centrum Onkologii, Pulmonologii i Hematologii
Pl. Ludwika Hirszfelda 12, 53-413 Wrocław
tel.: (71) 368 96 01
www.dcopih.pl
Izerskie Centrum Pulmonologii i Chemioterapii Izer-Med.
ul. Sanatoryjna 1, 58-580 Szklarska Poręba
tel.: (75) 754 71 00
www.icpich.izer-med.com.pl
woj. lubelskie
Uniwersytecki Szpital Kliniczny nr 1 w Lublinie
ul. Stanisława Staszica 16, 20-081 Lublin
tel.: (81) 532 50 41
www.spsk1.lublin.pl
Wojewódzki Szpital Specjalistyczny im. S.K. Wyszyńskiego, SPZOZ w Lublinie
Al. Kraśnicka 100, 20-718 Lublin
tel.: (81) 537 42 34
www.szpital.lublin.pl
woj. lubuskie
Szpital Uniwersytecki im. Karola Marcinkowskiego w Zielonej Górze
ul. Zyty 26, 65-046 Zielona Góra
tel.: 683 296 200
www.szpital.zgora.pl
woj. łódzkie
Wojewódzkie Wielospecjalistyczne Centrum Onkologii i Traumatologii im. M. Kopernika w Łodzi
ul. Pabianicka 62, 93-513 Łódź
tel.: (42) 689 52 00
www.kopernik.lodz.pl
Specjalistyczny Szpital Onkologiczny Tomaszów Mazowiecki/Grupa Nu-med
ul. Jana Pawła II 35, 97-200 Tomaszów Mazowiecki
tel.: (44) 786 81 00
www.nu-med.pl
woj. małopolskie
Szpital Uniwersytecki w Krakowie
ul. Kopernika 36, 31-501 Kraków
tel.: (12) 400 10 00
www.su.krakow.pl
woj. mazowieckie
Szpital Grochowski
ul. Młynarska 46, 00-171 Warszawa
tel.: (22) 515 26 09
www.grochowski.waw.pl
Państwowy Instytut Medyczny MSWiA
ul. Wołoska 137, 02-507 Warszawa
tel.: (47) 722 15 52
www.gov.pl/web/cskmswia
Narodowy Instytut Onkologii im. M. Skłodowskiej-Curie Państwowy Instytut Badawczy
ul. W.K. Roentgena 5, 02-781 Warszawa
tel.:
a href=”http://www.nio.gov.pl/”>www.nio.gov.pl
Uniwersyteckie Centrum Kliniczne Warszawskiego Uniwersytetu Medycznego
ul. Banacha 1A, 02-097 Warszawa
tel.: (22) 546 20 00
https://uckwum.pl
woj. opolskie
Opolskie Centrum Onkologii im. prof. T. Koszarowskiego
ul. Katowicka 66a, 45-061 Opole
tel.: (77) 441 6004-05
www.onkologia.opole.pl
woj. podkarpackie
Wojewódzki Szpital im. Św. Ojca Pio w Przemyślu
ul. Monte Cassino 1, 37-700 Przemyśl
tel.: (16) 736 05 00
www.wszp.pl
woj. podlaskie
Białostockie Centrum Onkologii im. M. Skłodoskiej-Curie
ul. Ogrodowa 12, 15-027 Białystok
tel.: (85) 678 41 12
www.onkologia.bialystok.pl
woj. pomorskie
Uniwersyteckie Centrum Kliniczne
ul. Dębinki 7, 80-952 Gdańsk
tel.: (58) 727 05 05
www.uck.pl
woj. śląskie
Narodowy Instytut Onkologii w Gliwicach
ul. Wybrzeże Armii Krajowej 15, 44-102 Gliwice
tel.: (32) 278 88 88
www.gliwice.nio.gov.pl
Wojewodzki Szpital Specjalistyczny Nr 4 W Bytomiu
Al. Legionów 10, 41-902 Bytom
tel.: (32) 281 02 71
www.szpital4.bytom.pl
woj. warmińsko-mazurskie
Szpital Kliniczny MZWiA z Warmińsko-Mazurskim Centrum Onkologii w Olsztynie
Aleja Wojska Polskiego 37, 10-228 Olsztyn
tel.: (89) 539 80 00
www.poliklinika.net
woj. wielkopolskie
Uniwersytecki Szpital Kliniczny w Poznaniu
ul. Przybyszewskiego 49, 60-355 Poznań
tel.: (61) 869 11 00
www.skhs.pl
Wielkopolskie Centrum Onkologii
ul. Garbary 15, 61- 866 Poznań
tel.: (61) 885 05 00
www.wco.pl
woj. zachodniopomorskie
Samodzielny Publiczny Wojewódzki Szpital Zespolony w Szczecinie
ul. Arkońska 4, 71-455 Szczecin
tel.: (91) 442 72 00
www.spwsz.szczecin.pl
Samodzielny Publiczny Szpital Kliniczny nr 1 im. prof. T. Sokołowskiego Pomorskiego Uniwersytetu Medycznego
ul. Unii Lubelskiej 1, 71-252 Szczecin
tel.: (91) 425 30 00
www.spsk1.szn.pl
Zachodniopomorskie Centrum Onkologii
ul. Strzałowska 22, 71-730 Szczecin
tel.: (91) 425 14 10
onkologia.szczecin.pl
Poznaj moją historię
Historia Ilony

Mam na imię Ilona, za moment kończę 43 lata i od 15-tu lat mieszkam w Anglii. 3 lata temu zdiagnozowano u mnie raka dróg żółciowych, chorobę o której istnieniu nie wiedziałam ani ja, ani nikt z moich bliskich, znajomych, ani kolegów.
Moja choroba, jak zresztą u wielu osób, rozwinęła się na długo przed oficjalną diagnozą. Może umknęło mi, kiedy dokładnie zaczęłam się źle czuć. W 2018 przestałam pić alkohol, bo powodował reakcje alergiczną, ale nie powiązałam tego zupełnie z wątrobą. Pojawiły się też bóle w dolnej części pleców. Nie mocne, ale trwające po kilka dni, uporczywe. Przychodziły raz na 2-3 miesiące i właściwie jakoś parę dni przed miesiączką, więc też nie myślałam o nich inaczej niż o zespole napięcia przedmiesiączkowego. Wykluczyłam wszystko inne, ale pomyślałam, że być może to również przez kiepski materac, na którym śpię. Bóle trwały, ale życie też toczyło się dalej. Dostałam nową pracę, przeprowadziłam się do nowego mieszkania, kupiłam nowy materac.
W 2019 r. powiedziałam koleżance, że boli mnie krzyż i prawa część brzucha, po stronie wątroby. Kazała mi od razu umówić się na wizytę do lekarza, co zresztą zrobiłam i już następnego dnia miałam poradę telefoniczną, w trakcie której doszliśmy z lekarzem do wniosku, że to pewnie niestrawność. Chociaż zaznaczył, że dobrze by było mnie zobaczyć. Bóle przeszły a z nimi myśl, że powinnam się jednak zgłosić na jakieś badanie, albo chociaż po poradę w przychodni.
Przeszło mi przez myśl, że to może rak. Rak wątroby. Wciąż miałam w pamięci Davida Bowie i jego Lazarusa – pośmiertnie wyprodukowany musical, który miałam okazję zobaczyć. Na jednym ze zdjęć zrobionych niedługo przed śmiercią, Bowie trzyma się za prawą stronę tułowia, kładąc rękę na prawdopodobnie bolącej wątrobie. Bowie zmarł na raka wątroby, ale właściwie co mnie z nim łączyło, oprócz bólu? Postanowiłam jednak sprawdzić w internecie, jakie w razie czego, są objawy tego nowotworu: ból brzucha, nudności, gorączka, zmęczenie, swędzenie skóry, żółtaczka. A czynniki ryzyka? Nie piłam, palenie rzuciłam na dobre w 2017 roku, byłam przed 40-tką, prowadziłam aktywny tryb życia, nie byłam otyła, nie jadłam mięsa, a w rodzinie wszyscy byli zdrowi. Nikt w bliskiej rodzinie nie miał raka, wszyscy żyli, włącznie z moją babcią, ostatni pogrzeb mieliśmy 20 lat temu…
Funkcjonowałam z przychodzącym i odchodzącym bólem przez 2019 rok, a potem przez pandemię i lockdown. W sierpniu 2020 r. poczułam zmęczenie. Zaczęłam biegać kilka razy w tygodniu, żeby się upewnić, że nie zasiedziałam się w pandemii. Ale robiłam to coraz słabiej zamiast coraz lepiej. Czułam się zmęczona i któregoś dnia miałam stan podgorączkowy. To dziwne w środku lata, ale minęło, zrobiłam sobie nawet test na Covid – wyszedł negatywny.
Którejś nocy przyszedł silny ból pleców. Tak silny, że nie mogłam spać, a nad ranem zwymiotowałam. Zadzwoniłam do przychodni, bo porady przez telefon stały się standardem wprowadzonym w czasie pandemii. Opowiedziałam lekarce o moich objawach, do których w kolejnych dniach doszedł jeszcze na ciemno zabarwiony mocz i kał koloru jasnobeżowego, co było niezbyt normalne, jak dla mnie. Pani Doktor poleciła mi iść na SOR, na badania. Poszłam jeszcze tego samego dnia, a tam lekarz wyłącznie na podstawie badania krwi postawił diagnozę: najprawdopodobniej kamienie żółciowe, kał na pewno nie odbarwiony (pokazałam mu zdjęcie w komórce), a USG nie jest konieczne, do widzenia.
Po dwóch tygodniach i utracie 5 kg, z żółtaczką, byłam z powrotem na SOR. Wtedy usłyszałam, że mam coś w wątrobie.
– Musimy zrobić jeszcze parę testów i zahamować żółtaczkę. Będziesz przeniesiona do innego szpitala.
– Ale co mi jest?
– Masz coś w wątrobie.
To było tyle, od razu pomyślałam, że to rak, albo jakiś inny guz. Po przeniesieniu mnie do innego szpitala zrobiono mi jeszcze rezonans i PET. Lekarz prowadzący przysunął sobie krzesło koło mojego łóżka, zdjął maseczkę, mimo, że wciąż trwał Covid.
– Myślimy, że to rak. Rak dróg żółciowych. Normalnie występuje u osób starszych, ale widzieliśmy sporo przypadków u osób w Twoim wieku, a nawet młodszych.
Okazało się, że żółtaczka spowodowana była zablokowaniem dróg żółciowych przez guza. Nie powiedziano mi jak duży był to guz jedynie, że jest tylko jeden. PET nic nie wykazał, więc stwierdzono, że nie mam przerzutów. Rak nie nadawał się jednak do wycięcia: za duży, za blisko głównej żyły. Wstawili mi plastikowy stent, żeby udrożnić drogi, następnym krokiem miała być chemia, a potem, jeśli to zadziała i guz się zmniejszy, operacja.
Po dwóch tygodniach w szpitalu wróciłam do domu. Na wizytę u onkologa musiałam trochę poczekać, ale pierwszą chemioterapię miałam tuż przed świętami Bożego Narodzenia.
Czekałam na rezultat podawanej chemii, a po drodze został wymieniony stent, ponieważ wdała się infekcja.
W lutym wykonano mi kolejne badanie. Kiedy zadzwoniła do mnie pielęgniarka, a nie onkolog, trochę się zdziwiłam. To był mój szczęśliwy dzień, czułam się jakbym wygrała loterię, bo okazało się, że widzieli moje wyniki i zaproponowali mi operację. Zaproszono mnie na konsultację, podczas której wyjaśniono mi na czym miała polegać operacja, jakie niosła za sobą ryzyko, a jakie ewentualne powikłania.
Operację miałam 31-go marca 2021. Poszła sprawnie i wycięto mi całego guza. Wszystko, razem z woreczkiem żółciowym, częścią głównego przewodu żółciowego (wątrobę podpięto bezpośrednio do dwunastnicy) i kilkoma węzłami chłonnymi, które przekazano do dalszych badań.
Rekonwalescencja przebiegała bez żadnych większych zmartwień, jeśli nie liczyć bardzo małej infekcji pooperacyjnej, z którą szybko się uporano. Zdecydowałam się na po-operacyjną chemioterapię, w razie, gdyby komórki rakowe gdzieś się jeszcze uchowały. Zaczęłam ją szybko i skończyłam w sierpniu.
Ta runda chemioterapii jednak mnie zmiotła. Zrobiłam się bardzo zmęczona, miałam tzw. chemobrain. Stałam się bardzo wolna, często nie rozumiałam co się do mnie mówi, albo zapominałam słów. Stałam się zapominalska i nie mogłam prowadzić normalnych interakcji z innymi. Spotkania ze znajomymi, zwłaszcza w większym gronie stały się torturą. Do tego doszła utrata słuchu (na szczęście nie na stałe, ale utrzymywała się przez kilka miesięcy), wczesna menopauza i rany w ustach.
Po zakończeniu chemioterapii długo dochodziłam do siebie. Głównie psychicznie. Nie mogłam odnaleźć się w nowej rzeczywistości „po raku”. Z jednej strony była siła i nadzieja, że udało mi się pokonać raka dróg żółciowych, bo niewielu osobom się to udaje. Niewiele osób ma też szansę na operację, a ja ją dostałam. Przyszło też poczucie winy, że ja miałam to szczęście, że ja przeżyłam. Z drugiej strony był strach i zwątpienie. To rak, którego bardzo rzadko udaje się pokonać. Z każdym kontrolnym badaniem myślałam: Czy to już? Czy już jest nawrót? Przez Internet poznałam kilka osób, które też miały RDŻ. Jedną z nich była Charlotte, której nawrót choroby po operacji nastąpił bardzo szybko, jeszcze w trakcie chemioterapii. Wówczas pojawiło się kolejne pytanie: Czy ja też znajdę się w tej grupie pacjentów?
Trochę ponad rok od operacji pojawiły się 3 nowe guzy. Małe, ale wyglądało na to, że rak wrócił. Po raz pierwszy wtedy poczułam, jak robi mi się gorąco i łzy napłynęły mi do oczu. Czułam się dobrze i chyba ta różnica tego jak się czuję i tego co się dzieje wewnątrz mojego organizmu, ten dysonans sprawił, że tak zareagowałam.
– Czy mogą operować raz jeszcze? Nie. No, może, jeśli chemia zadziała.
Wiedzieliśmy, że chemia zadziałała za pierwszym razem, więc zdecydowałam się wziąć ją jeszcze raz. Po dwóch miesiącach kolejny skan. Guzy urosły. Wciąż były małe, ale nie nastawiałam się na taką wiadomość. Co dalej? Wiedziałam, że kolejnym krokiem normalnie byłaby kolejna chemioterapia. Koniec drogi. Chyba, że mam mutację genu FGFR, wtedy mogłabym wziąć lek, który kilka miesięcy wcześniej został zatwierdzony do stosowania u pacjentów z RDŻ w Wielkiej Brytanii. Poprosiłam o badania genetyczne. W międzyczasie dowiedziałam się, że są badania kliniczne nowego leku, które prowadził mój onkolog. Zostałam zakwalifikowana i zaczęłam brać nowy lek. Zaletą było to, że był w tabletkach, wadą, że nie wiadomo było nawet czy działa i jaka jest częstotliwość występowania skutków ubocznych. Tych nie miałam sporo, ale straciłam odczuwanie normalnego smaku. Wszystko było słone i kwaśne, nie mogłam jeść słodyczy, bo smakowały okropnie. Zaczęłam być też coraz bardziej zmęczona.
Wyniki krwi w kierunku zmian genetycznych (tzw. płynna biopsja) nie wykazały żadnych widocznych mutacji. Potem przyszły wyniki pierwszego skanu. Rak urósł, więc lek nie zadziałał. Załamałam się, bo wiedziałam, że musimy go powstrzymać, a nie wiedziałam, czy mam jeszcze jakieś inne opcje. Na szczęście czułam się w miarę dobrze i mogłam wziąć udział w kolejnym badaniu klinicznym. Tym razem immunoterapia. Również w tabletkach, poza tym onkolog chciał zrobić płynną biopsję jeszcze raz. Znów miałam minimalne skutki uboczne, poza narastającym zmęczeniem. I znów po dwóch miesiącach dostałam wiadomość: guzy rosną, więc i ten lek nie działa. Wiedziałam, że badania kliniczne często kończą się niepowodzeniem – dla pacjentów i dla firm farmaceutycznych, które prowadzą badania nad nowymi terapiami, nowymi lekami.
Dostałam wynik biopsji i po raz pierwszy, odkąd lekarze wiedzieli, że mam raka dróg żółciowych dostałam odpowiedź co powoduje u mnie raka. Okazało się, że mam trzy mutacje (w różnym stopniu) genów: IDH1, BRAF i ARID1A. Mój onkolog nie miał dla mnie jednak pocieszających informacji. Istnieje lek, który nacelowany jest na mutacje IDH1, ale nie jest dostępny w Wielkiej Brytanii i kosztuje majątek.
Zaczęłam kombinować, bo w tym momencie poczułam, że właściwie jestem pozostawiona sama sobie. Czy mam zacząć zbiórkę i kupić ten lek? Czy mam jeszcze szukać innych badań klinicznych, mimo, że te dwa poprzednie badania kliniczne nie odniosły rezultatu? Byłam w kropce.
Jednak szczęście się do mnie uśmiechnęło. Okazało się, że firma farmaceutyczna produkująca lek, który celuje w IDH1, stara się o licencję i dofinansowanie w NHS, odpowiednika polskiego NFZ. Lek będzie podany małej liczbie wybranych pacjentów na zasadzie wczesnego dostępu. Po paru miesiącach w stresie, e-mailach do kilku szpitali, rozmów telefonicznych i paru wizyt okazało się, że jest miejsce dla mnie w tym programie. Zaczęłam przyjmować lek dwa miesiące temu. Właściwie znów nie mam żadnych efektów ubocznych. Ból spowodowany przez raka jednak się nasila. Bazowy skan TK wykazał, że guzy, które rok temu były małe, urosły do ok 6 cm. Do tego węzeł chłonny po prawej stronie też trochę urósł, co wskazuje na przerzut do otrzewnej. Skan mający na celu pokazanie, czy lek działa miałam pod koniec listopada 2023 r. i czekam na wyniki.
Moja choroba dalej trwa, niezależnie od wyniku. Chcę być dobrej myśli, choć po trzech latach przychodzi mi to z trudem. Na szczęście mam wsparcie rodziny, przyjaciół, wsparcie psychologa i moją wiarę. To chyba dla mnie najważniejsze.
Historia Marzeny

Mam na imię Marzena, mam 45 lat, wspaniałego męża i troje dzieci, najlepszych! Mam też raka, jednego z najgorszych, rzadkiego, bardzo złośliwego, źle rokującego…RDŻ (rak dróg żółciowych).
Zawsze byłam szczupła, biegam (mam na koncie kilka półmaratonów) pływam, jeżdżę na rowerze. Nie palę papierosów, ale jestem uzależniona od kawy 🙂 Może brzmi trochę śmiesznie ale całe życie borykam się z niskim ciśnieniem i bez kawy po prostu nie jestem w stanie funkcjonować. Lubię podróżować i chodzić po górach i czerwone wino lubię, w piątek wieczorem.
Nie wiem jak długo i podstępnie mógł rozwijać się we mnie rak. USG robiłam tylko przy okazji ciąży. Błąd!!! Teraz, kiedy patrzę wstecz przypominam sobie o objawach, które mogły świadczyć o rozwoju RDŻ, ale ja je bagatelizowałam. Już w trakcie pandemii pobolewała mnie prawa ręka (na pewno na niej spałam), anemia (to przez obfite miesiączki), dyskomfort w brzuchu po grillu (cóż, po czterdziestce już nie to samo trawienie) …. tak to sobie tłumaczyłam.
W maju 2022 r. zaczęłam wyczuwać w brzuchu coś twardego. Mój lekarz POZ wysłał mnie na USG. Później wszystko działo się szybko, bo sprawa okazała się poważna. To, że mam raka dowiedziałam się w dniu rocznicy ślubu 21 lipca, lekarz przekazał mi tę informację na podstawie wyniku z rezonansu. Było bardzo źle – guz bardzo duży, prawdopodobnie nieresekcyjny, podejrzenie nacieku na nerki, zajęcie węzłów chłonnych, same znaki zapytania. Wynik biopsji tylko potwierdził, że to rak.
Zaczęłam szukać pomocy, wśród znajomych, lekarzy, w Internecie. Rodzina i przyjaciele bardzo mi wtedy pomogli. Z jednej strony działałam, konsultowałam, miałam w sobie sporo siły z drugiej jednak zaczęłam się żegnać, z dziećmi zwłaszcza. Dokończyłam niezałatwione sprawy, zostawione na kiedyś. Najważniejsze było znaleźć chirurga, który odważyłby się podjąć operacji – tak mi radzili lekarze, znajomi. Po ok. sześciu miesiącach od mojej wizyty w POZ znaleźliśmy takie chirurga 600 km od mojego miejsca zamieszkania. Pojechałam. Dowiedziałam się dokładnie jak będzie przebiegać operacja, że będzie długa i trudna i że moje szanse na powodzenie wynoszą 50%.
Zaufałam i było warto! Ten lekarz uratował mi życie!!! Czuję wdzięczność, a życie i radość z każdego dnia zaczęły smakować wyśmienicie. To nic, że wycięto mi cały prawy płat wątroby z woreczkiem. Ona szybko odrosła. Byłam Prometeuszem!!! Szybko i bez komplikacji doszłam do siebie, rana szybko się zagoiła. Podpisałam też zgodę na publikację mojego przypadku, podobno ciekawy. Bardzo się cieszyłam, że nie było nacieków, że w węzłach chłonnych nie znaleziono komórek nowotworowych. Teraz pozostało znaleźć dobrego onkologa, który doradziłby mi w zakresie chemioterapii, żeby zniszczyć ewentualne rozsiewy.
Kapecytabinę zaczęłam przyjmować dwa miesiące po operacji. Chemioterapię zniosłam dobrze. Myślałam, że wyłysieję, że będę miała biegunki i wymioty. Nic takiego się jednak nie działo. Najgorzej wspominam bóle brzucha, słabość, nadmierną senność, spory spadek poziomu żelaza, anemię. Bardzo pomogły mi kroplówki z żelazem, które dostałam w Instytucie, szybko postawiły mnie na nogi. Oprócz tego, że spałam po kilkanaście godzin dziennie, funkcjonowałam normalnie, po leki jeździłam sama, samochodem co trzy tygodnie do Gliwic. Byłam bardzo dzielna. W maju zakończyłam chemioterapię a już dwa miesiące później czułam się znów wspaniale, jak kiedyś – ZDROWA.
Uznałam, że powinnam o siebie teraz bardzo dbać, poszukałam w swoim mieście dietetyk kliniczną. To był dobry krok! Pani dietetyk ułożyła mi indywidualny jadłospis z wielką dokładnością. Wiem na ile tłuszczu, białka, węglowodanów mogę sobie pozwolić. Co jeść, czego unikać. Bardzo mi pomogła. Teraz byłam zdrowa, dobrze odżywiona, zabezpieczona przed nawrotem, bo brałam chemię.
Niestety, tym zdrowiem cieszyłam się do października. W listopadzie, na podstawie wyniku z rezonansu wyszło podejrzenie wznowy. Nie uwierzyłam w to! – Jak to, przecież w badaniu PET z sierpnia nic nie wyszło. To niemożliwe!!! Ale z drugiej strony nie bez powodu robią mi rezonans tak często…wcześniej się nad tym nie zastanawiałam.
Wynik ostatniego rezonansu polecono skonsultować z chirurgiem. Oprócz tego otrzymałam skierowanie w sprawie konsultacji co do ewentualnego leczenia systemowego do kliniki w Warszawie. Na razie wiem, że moja wznowa jest „niechirurgiczna”. Jeśli chodzi o leczenie systemowe na razie też za wcześnie.
Boję się, że nie ma dla mnie leczenia. I choć mam bardzo dobrych lekarzy obok siebie to wymyślam czarne scenariusze. Czasem nie wierzę w swój nawrót, czasem czuję gniew. Toczę walkę sama ze sobą. Najgorsze jest czekanie. Muszę zaufać i cierpliwie czekać. Czy mam jakieś możliwości leczenia jeszcze???
Czekam na wynik ostatniego rezonansu, na którym byłam w piątek. Długo czekać nie muszę, bo na odczyt jadę już 17 stycznia. Strach czasem paraliżuje, zaczynam odczuwać fizyczne skutki stresu, ciągłego napięcia. Chciałabym wiedzieć ile czasu mi zostało, żeby go najlepiej zaplanować i wykorzystać. Mąż podsuwa mi wykresy z wyników amerykańskich badań z których wynika, że jeszcze pożyję…
Rodzina nie wie o wznowie. W święta uciekłam z mężem i dziećmi na Maltę.
Czekam…
Dzieci obiecały, że co roku będą robić USG jamy brzusznej.
* Przedstawione historie pacjentów i ich ścieżki leczenia są indywidualne i ustalane we współpracy z lekarzem prowadzącym.
Zdiagnozowano u Ciebie raka dróg żółciowych? Sprawdź, co to dla Ciebie oznacza!
Poniżej znajdziesz dokument zawierający listę przykładowych pytań do lekarza –
wybierz te, które Twoim zdaniem pomogą Ci lepiej zrozumieć postawioną diagnozę i plan leczenia.
Dieta
Jak za pomocą diety i zmiany stylu życia zmniejszyć ryzyko zachorowania na nowotwory przewodu pokarmowego
Niedożywienie u chorych na nowotwory złośliwe przewodu pokarmowego (NZPP) występuje rzadko i dotyczy głównie chorych z zaawansowaną postacią choroby. Zdecydowanie częściej u chorych na NZPP spotykamy się z problemem nadwagi i otyłości, który odzwierciedla nasilenie tego problemu w populacji polskiej. Badanie CBOS z 2019 r. wskazuje, że 59% dorosłych Polaków ma nadmierną masę ciała (38% ma nadwagę, 21% otyłość). Według raportu WHO z 2016 r. w Polsce nadwaga (BMI 25‒29,9 kg/m2) u kobiet występuje w ok. 28%, u mężczyzn w ok. 41%, zaś otyłość (BMI>30 kg/m2) odpowiednio dla płci w ok. 22% i ok. 24%. W Stanach Zjednoczonych Ameryki szacuje się, że aż 100.000 zachorowań na raka można by uniknąć gdyby Amerykanie pozbyli się nadmiarowych kilogramów.
Dla wielu nowotworów, w tym dla nowotworów złośliwych przewodu pokarmowego otyłość to niezależny czynnik ryzyka zachorowania. Szacuje się, że dla NZPP to ryzyko wynosi od 20-40%. Inne czynniki ryzyka dla NZPP związane z dietą i stylem życia to alkohol oraz siedzący tryb życia.
Zatem leczenie nadwagi i otyłości to pierwszy krok do zmniejszenia ryzyka zachorowania na NZPP.
Dieta w profilaktyce pierwotnej nowotworów złośliwych i otyłości
Rekomenduje się dietę śródziemnomorską, bogatą w warzywa, owoce, orzechy, produkty pełnoziarniste, warzywa strączkowe, oliwę z oliwek oraz ryby i owoce morze. Można się również odwołać do „New American Plate” („nowy amerykański rozkład posiłków na talerzu”), według American Institute for Cancer Research, który zakłada, że 2/3 na talerzu powinny stanowić produkty roślinne, w tym pełne ziarna, orzechy i strączkowe, a 1/3 to źródła białka z niską zawartością tłuszczów (ryby, drób). Zaleca się redukcję czerwonego mięsa do 300‒500 g mięsa czerwonego na tydzień. Szczególnie należy ograniczyć mięso czerwone w formie przetworzonej (wyroby wędliniarskie) <50g na tydzień.
Bez względu na to, czy wybierzemy model żywienia typowy dla basenu Morza Śródziemnego, czy model amerykański, warto mieć na uwadze, aby nasza dieta była bogata w produkty o udowodnionym potencjale zmniejszającym ryzyko zachorowania na nowotwór złośliwy, do których należą związki zebrane w tabeli 1. (Shanmugam, Muthu K., et al. „Cancer prevention and therapy through the modulation of transcription factors by bioactive natural compounds.” Seminars in cancer biology. Vol. 40. Academic Press, 2016).
Tabela 1. Wybrane związki antyoksydacyjne i ich potencjał antynowotworowy
| Klasa związków | Przykłady związków | Źródła | Aktywność antynowotworowa |
| Karotenoidy | α-karoten, β-karoten, likopen, β-kryptoksantyna, luteina, astaksantyna | żółto-pomarańczowe oraz ciemnozielone warzywa i owoce, szczególnie marchew, pomidory, dynia | aktywność antyoksydacyjna, modulacja metabolizmu kancerogenów, inhibicja komórkowej proliferacji, inhibicja ekspresji onkogenów, modulacja układu immunologicznego, hamowanie promocji guza |
Polifenole
| kwasy fenolowe, kwas hydroksycynamonowy (kurkumina) katechiny, flawony, resweratrol | winogrona, zielona herbata, cynamon, kurkuma truskawki i owoce czerwone, borówki | hamowanie tworzenia adduktów DNA, inhibicja proliferacji komórkowej, indukcja apoptozy, modulacja układu immunologicznego |
| Organiczne związki siarki | siarczek diallilu, disiarczek diallilu | Czosnek i cebule, warzywa krzyżowe | wzrost aktywności enzymów II fazy, inhibicja proliferacji komórkowej, zmiana metabolizmu hormonów steroidowych, inhibicja aktywności dekarboksylazy ornityny |
| Fitoestrogeny | izoflawony (genisteina, daidzeina), lignany | nasiona soi, w szczególności produkty sojowe fermentowane | wpływ na metabolizm estrogenów, spadek aktywności kinazy tyrozynowej, indukcja apoptozy |
| Terpeny | monoterpeny (limonen), seskwiterpeny (farnezol) | Cytrusy, Herbata z lipy
| wzrost aktywności enzymów II fazy, indukcja apoptozy |
| Glukozynolany, izotiocyjaniany, indole | sulforafan, indolo-3-karbinol, izotiocyjanian fenyloetylu | warzywa krzyżowe (różne rodzaje kapusty, rzodkwie, brokuły, kalafiory) | wzrost aktywności enzymów II fazy, indukcja apoptozy, inhibicja adhezji oraz inwazji komórkowej |
Relatywnie prosty trick do zastosowania w codziennej diecie, to reguła 5 kolorów.
5 różnych grup kolorystycznych w świecie roślinnym reprezentuje liczne prozdrowotne składniki niezbędne dla prawidłowego funkcjonowania ludzkiego organizmu, w większości wymienione w tabeli 1. Jeśli sięgamy po nie regularnie, możemy mieć pewność, że bez skomplikowanych obliczeń dostarczymy organizmowi witamin rozpuszczalnych w wodzie, niektórych pierwiastków śladowych i innych związków bioaktywnych.
Starajmy się, aby każdego dnia na naszym talerzu pojawiły się owoce i warzywa z 5 grup kolorystycznych:
- zielone: wszelkie warzywa zielonoliściaste: kapusty, sałaty, szpinak, jarmuż, zielone jabłka, zielona papryka, cukinia i wiele innych
- żółto-pomarańczowe: marchew, pomarańcze, papryka, mango, jabłka, gruszki, dynia,
- czerwone: większość owoców jagodowych, papryka, jabłka, pomidory,
- fioletowe: rzodkiewki, bakłażany, buraki, czarna porzeczka, jagody, borówki, ciemne winogrona,
- białe: czosnek, cebule, pory.
Dorosły człowiek powinien zjadać przynajmniej 500 g warzyw na dobę i 2 niewielkie porcje owoców. Cel ten jest bardzo prosty do osiągnięcia przy sięganiu do różnych grup kolorystycznych produktów roślinnych. Dla przykładu jeśli w skali doby zjemy: 1 niewielkie jabłko i pół szklanki borówek, 1 pomidor, porcję sałaty z różnych liści z dodatkiem marchwi, cebuli i ziół, pół papryki czerwonej i 2-3 rzodkiewki, spełniliśmy zasady diety 5 kolorów.
Ważne jest nie tylko, jakie produkty wybieramy, ale również jakie produkty należy ograniczyć i jakie nawyki żywieniowe eliminować. Warto stosować się do poniższych zaleceń.
- Ogranicz spożycie węglowodanów prostych, tłuszczów nasyconych oraz kwasów nienasyconych z rodziny omega-6. Nadmiar tych produktów to nadmiar energii prowadzący do nadwagi i otyłości. Dodatkowo mają one prozapalny potencjał. W tej grupie znajdziemy takie produkty jak: słodycze, słodkie napoje, cukier biały, wypieki z wysokoprzetworzonej mąki pszennej (ciasta, białe chleby i bułki). Tłuszcze, które powinny być ograniczane, to masło, smalec, olej słonecznikowy, dyniowy, kukurydziany, arachidowy, orzechy arachidowe.
- Tłuszcze zalecane to oliwa z oliwek, olej rzepakowy, olej lniany, awokado, migdały, orzechy włoskie.
- Kontroluj niedobory! Zadbaj o prawidłową podaż błonnika. To niezbędna odżywka dla twojej mikroflory jelitowej ‒ potrzebujemy 25‒40 g błonnika na dobę. W prosty sposób osiągniesz ten cel jedząc codziennie 2 kromki chleba pełnoziarnistego i pół szklanki dowolnej kaszy. Zapytaj swojego lekarza, czy zasadne jest w twoim wypadku wykonanie badań w kierunku niedoboru żelaza, cynku, witaminy D i innych witamin. W przypadku rozpoznania niedoboru, włącz suplementację wg zaleceń lekarskich.
- Zwracaj uwagę na źródło pochodzenia żywności (hodowle i uprawy naturalne vs przemysłowe), o ile to możliwy postaw na uprawy ekologiczne.
- Przyjrzyj się sposobowi obróbki żywności: grillowanie, smażenie, wędzenie są niezalecane. Wybieraj produkty świeże, nieprzetworzone, bez dodatków konserwujących, wpływających na smak lub konsystencję. Wybieraj produkty gotowane lub duszone. Jedz proste posiłki – przyjmij zasadę: „Nie jem niczego, co ma w składzie powyżej pięciu składników”. Czytaj etykiety produktów spożywczych.
- Zwróć uwagę na sposób przechowywania żywności ‒ żywność zepsuta, zanieczyszczona pleśnią, produkty wielokrotnie odgrzewane są groźne dla zdrowia.
- Uważaj na spożycie alkoholu. Każda redukcja spożycia alkoholu to dobry krok w kierunku zdrowia. Nie przekraczaj ilości 10‒12g etanolu na dobę, co odpowiada porcji piwa 330 ml lub kieliszkowi wina 150 ml.
- Staraj się nie objadać wieczorem. Jedz pożywne śniadania, staraj się zjadać 4 niewielkie posiłki dziennie: śniadanie, II śniadanie, lunch, lekka kolacja. Uważaj na przekąski dostarczające nadmiernej energii: chipsy, orzechy, owoce suszone, słodycze, słodkie napoje, soki przecierowe, nektary owocowe.
- Nie stosuj na własną rękę suplementów diety, witamin, ziół. Niektóre produkty, jak sok z grejpfruta, granata, żeń-szeń mogą wchodzić w groźne interakcje lekowe. W razie wątpliwości pytaj lekarza lub dietetyka klinicznego.
Bazując na zaleceniach towarzystw naukowych (ESPEN – European Society for Clinical Nutrition and Metabolism, POLSPEN – Polskie Towarzystwo Żywienia Pozajelitowego, Dojelitowego i Metabolizmu) dotyczących żywienia klinicznego pacjentów z chorobą nowotworową, zaleca się utrzymywanie prawidłowej masy ciała (BMI 18,5-24,9 kg/m2) i włączenie regularnej aktywności fizycznej ‒ minimum 150 minut w tygodniu. Aktywność fizyczną można podzielić na sesje 5 razy w tygodniu po 30 minut, złożone z wysiłku aerobowego i ćwiczeń oporowych, z osiągnięciem submaksymalnego poziomu tętna w trakcie wysiłku.
Kluczowe w profilaktyce, prewencji wtórnej, jak i w aktywnej terapii wszystkich nowotworów złośliwych jest rzucenie palenia tytoniu. Nikotynizm skraca życie, zwiększa częstość powikłań chirurgicznych i infekcyjnych, zwiększa koszty leczenia.
Jeśli potrzebujesz pomocy dietetyka klinicznego, zapraszamy na konsultację do nas!
Wykwalifikowany zespół lekarsko-dietetyczny pomoże dobrać dietę, suplementy, ustali wskazania do żywienia sztucznego, oceni stan odżywienia i ewentualne niedobory.
Poradę dietetyczną możesz uzyskać w Narodowym Instytucie Onkologii w Warszawie,
ul. Roentgena 5 w Poradni Chorób Metabolicznych.
Do Poradni wymagane jest skierowanie.
Poradnia znajduję się w gabinecie 133 przy wejściu „E”.
Do Poradni należy się wcześniej zapisać w rejestracji głównej lub pod numerem telefonu 22 546 20 00
Zapraszamy!
Artykuł powstał we współpracy z dr n. med. Aleksandrą Kapałą, Kierownik Działu Dietetyki Klinicznej w Narodowym Instytucie Onkologii im. M. Skłodowskiej-Curie w Warszawie, Państwowy Instytut Badawczy

Dieta, sposób żywienia jako prewencja raka dróg żółciowych
Iga Rawicka Prezes Fundacji EuropaColon Polska w rozmowie z dr n. med. Aleksadrą Kapałą, Kierownik Kliniki Diagnostyki Onkologicznej, Kardioonkologii i Medycyny Paliatywnej oraz Kierownik Działu Żywienia Klinicznego Narodowego Instytutu Onkologii im. Marii Skłodowskiej-Curie Państwowego Instytutu Badawczego, o tym w jaki sposób można zapobiec rakowi dróg żółciowych stosując właściwą dietę i zdrowy styl życia.
Słuchaj na YouTube lub Spotify:
Problemy żywieniowe u chorych na raka dróg żółciowych
Na etapie aktywnego leczenia raka dróg żółciowych (RDŻ), czy to leczenia chirurgicznego czy systemowego, chory może doświadczać różnych dolegliwości z przewodu pokarmowego jak jadłowstręt, nudności i wymioty, biegunki, zaparcia, wzdęcia, ból. Ponadto, na różnym etapie choroby może dojść do żółtaczki, mogą również pojawić się cechy uszkodzenia wątroby do jej niewydolności włącznie, a także wodobrzusze i obrzęki. Na szczęście zdecydowana większość chorych na RDŻ może odżywiać się doustnie zwykłą, prawidłowo zbilansowaną dietą. Dopóki nie ma nasilonych dolegliwości, żółtaczki bądź cech uszkodzenia wątroby rekomenduje się dietę śródziemnomorską.
W przypadku obecności nudności i wymiotów, spadku apetytu i tendencji do biegunek zaleca się wprowadzenie diety łatwostrawnej, której podstawowe cechy to:
- eliminacja produktów ciężkostrawnych: smażonych, grillowanych, wędzonych, tłustych,
- ograniczenie produktów bogatych w błonnik nierozpuszczalny, a także warzyw wzdymających: kapustne, strączkowe, orzechy, produkty pełnoziarniste, grzyby, cebulowate,
- a dodatkowo w przypadku biegunek wybór produktów z niską zawartością laktozy, zamiana mleka krowiego/koziego na „mleka” roślinne: sojowe, ryżowe, owsiane, migdałowe.
Niedożywienie u chorych na RDŻ jest zjawiskiem rzadkim i zazwyczaj związanym z zaawansowaną chorobą. Niezamierzona utrata masy ciała (>5%) to sygnał, że należy rozpocząć interwencję żywieniową. Dietetyk kliniczny wyda stosowne zalecenia dotyczące diety oraz dobierze adekwatne suplementy diety (FSMP – food for special medical purpose). Od tego momentu zalecenia przybierają charakter indywidualny i bazują na wiodących objawach, typie stosowanego leczenia, dostępnych danych antropometrycznych i biochemicznych oraz biorą pod uwagę choroby współistniejące, np. cukrzycę czy zaburzoną funkcję nerek, obecność żółtaczki bądź cech uszkodzenia wątroby. Produkty typu FSMP to kompletne (lub nie) źródło pożywienia o znanym, precyzyjnie określonym składzie. Najczęściej proponujemy produkty z podwyższoną zawartością białka, jednakże gama tych produktów jest obecnie bardzo szeroka. W zależności od sytuacji klinicznej (cukrzyca, uszkodzona funkcja nerek, wątroby, trzustki, systemu odpornościowego czy zaburzone możliwości wchłaniania, żółtaczka) dietetyk kliniczny gwarantuje właściwy wybór FSMP.
W przypadku gdy zindywidualizowaną dietą wspartą FSMP nie udaje się zaspokoić w ponad 60% dobowego zapotrzebowania na energię i białko, należy rozważyć wskazania do żywienia sztucznego. W pierwszej kolejności zawsze rozważamy zasadność żywienia do przewodu pokarmowego przy użyciu diet przemysłowych (specjalne diety medyczne o kontrolowanym składzie). Jeśli wsparcie żywieniowe potrzebne jest na krótko (do 30 dni), wystarczy założyć zgłębnik nosowo-żołądkowy bądź nosowo-jelitowy. W przypadkach wymagających żywienia powyżej miesiąca zakładamy dostępy do żywienia zazwyczaj drogą endoskopową. Najczęściej to przezskórna endoskopowa gastrostomia, czyli PEG (percutaneous endoscopic gastrostomy). W szczególnych przypadkach używamy dostępu dojelitowego – mikrojejunostomii wytworzonej drogą chirurgiczną bądź endoskopową. Diety przemysłowe podawane do dostępów do przewodu pokarmowego mają różny skład i wartość odżywczą. W zdecydowanej większości sięgamy po diety o składzie standardowym, wysokobiałkowe i/lub wysokoenergetyczne. Warto pamiętać, że również diety dojelitowe oferowane są dla różnych grup pacjentów i uwzględniają różne wymagania związane z chorobą.
W przypadku gdy przewód pokarmowy nie jest dostępny, np. z powodu niedrożności czy ciężkiego zapalenia błony śluzowej, albo gdy żywienie dojelitowe nie jest tolerowane, albo jest niewystarczające, zaleca się żywienie drogą żył (żywienie pozajelitowe). Może ono być prowadzone drogą żył obwodowych (krótko, do 10 dni), bądź drogą żył centralnych – bezterminowo. W tej formie leczenia żywieniowego dostarczamy do krwioobiegu glukozę, aminokwasy, emulsje tłuszczowe, witaminy, pierwiastki śladowe, elektrolity i wodę w ilościach adekwatnych do bieżącego zapotrzebowania, wyników badań i sytuacji klinicznej. Żywienie pozajelitowe prowadzi lekarz, sama procedura wymaga szczegółowego nadzoru pod kątem powikłań takich jak zakażenia odcewnikowe, zakrzepica, zespół ponownego odżywienia, zaburzenia glikemii, gospodarki wodno-elektrolitowej czy kwasowo-zasadowej.
Niekiedy – w zależności od indywidualnej sytuacji pacjenta, łączymy metody żywienia, tak aby pokryć zapotrzebowanie dobowe na białko i energię.
Szczególne sytuacje kliniczne:
Żółtaczka. Uszkodzenie funkcji wątroby.
W zależności od przyczyny żółtaczki, postępowanie terapeutyczne, a także rokowanie są odmienne. Jeśli istnieje możliwość skutecznego protezowania dróg żółciowych i uzyskania odpływu żółci – żółtaczka będzie się stopniowo zmniejszała, a zalecenia żywieniowe będą rozszerzane do diety łatwostrawnej lub zwykłej. W przypadku gdy żółtaczka ma charakter trwały i jest wynikiem niepoddających się leczeniu zmian jak np. liczne przerzuty w wątrobie wówczas zalecenia będą bardziej restrykcyjne, patrz niżej. W przypadku uszkodzenia funkcji wątroby bez żółtaczki, a także w przypadku niewydolności wątroby, gdzie poza zwiększeniem aktywności enzymów wątrobowych występują zaburzenia krzepnięcia, hipoalbuminemia i hipoglikemia również bazujemy na diecie restrykcyjnej.
Na czym zatem polega dieta restrykcyjna w żółtaczce i niewydolności wątroby?
Należy wdrożyć zalecenia diety łatwostrawnej, a dodatkowo maksymalnie ograniczyć podaż tłuszczy i wspierać chorego FSMP beztłuszczowymi albo typu hepa. FSMP typu hepa mają specjalny skład. Zmieniono w nich zasoby aminokwasów. Usunięto aminokwasy aromatyczne, które są prekursorem dla toksyn powodujących śpiączkę wątrobową w niewydolności wątroby, a zastąpiono je aminokwasami rozgałęzionymi, które takich właściwości nie mają. Tłuszcze w preparatach hepa, to tłuszcze typu MCT (mediu-chain-triglycerides), które są bardzo łatwo przyswajalne i służą wątrobie jako źródło energii, jak glukoza. Powszechnie popełniany błąd to ograniczanie choremu źródeł węglowodanów prostych i białka, a tymczasem węglowodany proste mogą pokryć nawet 70% energii w diecie, zaś białko (mięso, ryby, białko jaja, nabiał) może być podawane choremu do czasu rozwoju śpiączki wątrobowej. Zaleca się zatem białe pieczywo, biały ryż i delikatne płatki, makarony, ziemniaki, miód, słodkie owoce, ciasta domowe jak biszkopty, herbatniki, bezy, nabiał niskotłuszczowy, soki i przeciery owocowe, gotowane warzywa korzeniowe i dyniowate, gotowane delikatne mięsa i ryby w sosie. Można dosładzać napoje, przyprawiać potrawy zgodnie z życzeniem chorego. Techniki kulinarne to gotowanie w wodzie i na parze, duszenie bez obsmażania, pieczenie w rękawie foliowym.
Jeśli potrzebujesz pomocy dietetyka klinicznego, zapraszamy na konsultację do nas!
Wykwalifikowany zespół lekarsko-dietetyczny pomoże dobrać dietę, suplementy, ustali wskazania do żywienia sztucznego, oceni stan odżywienia i ewentualne niedobory.
Poradę dietetyczną możesz uzyskać w Narodowym Instytucie Onkologii w Warszawie,
ul. Roentgena 5 w Poradni Chorób Metabolicznych.
Do Poradni wymagane jest skierowanie.
Poradnia znajduję się w gabinecie 133 przy wejściu „E”.
Do Poradni należy się wcześniej zapisać w rejestracji głównej lub pod numerem telefonu 22 546 20 00
Zapraszamy!
Artykuł powstał we współpracy z dr n. med. Aleksandrą Kapałą, Kierownik Działu Dietetyki Klinicznej w Narodowym Instytucie Onkologii im. M. Skłodowskiej-Curie w Warszawie, Państwowy Instytut Badawczy

Dieta jako wsparcie w trakcie leczenia raka dróg żółciowych
Iga Rawicka Prezes Fundacji EuropaColon Polska w rozmowie z dr n. med. Aleksadrą Kapałą, Kierownik Kliniki Diagnostyki Onkologicznej, Kardioonkologii i Medycyny Paliatywnej oraz Kierownik Działu Żywienia Klinicznego Narodowego Instytutu Onkologii im. Marii Skłodowskiej-Curie Państwowego Instytutu Badawczego, o tym w jaki sposób radzić sobie z ewentualną utratą masy ciała, która może dotyczyć 60% osób z rakiem dróg żółciowych.
Słuchaj na YouTube lub Spotify:
Wsparcie psychoonkologiczne

Samotność pacjentów z rakiem dróg żółciowych. Jak sobie z nią radzić?
Iga Rawicka Prezes Fundacji EuropaColon Polska w rozmowie z dr n. med. Mariolą Kosowicz, psycholożką, psychoonkolożką i psychoterapeutką, kierowniczką Poradni Zdrowia Psychicznego Narodowego Instytutu Onkologii – Państwowego Instytutu Badawczego im. Marii Skłodowskiej-Curie, na temat samotności pacjenta z rakiem dróg żółciowych.
Słuchaj na YouTube lub Spotify:
Organizator kampanii

Patronat
Konsultant krajowy ds. gastroenterologii


Mecenat kampanii

Udostępnione materiały powstały dzięki współpracy merytorycznej z dr n. med. Ewą Chmielowską,
Ordynator Pododdziału Chemioterapii i Oddziału Chemioterapii Jednodniowej
w Specjalistycznym Szpitalu Onkologicznym NU-MED w Tomaszowie Mazowieckim

